Ion sodium (Na⁺) : Cation formé par perte d'un électron par l'atome de sodium.
- Déterminer le numéro atomique Z (nombre de protons)
- Compter le nombre d'électrons dans l'ion
- Appliquer la formule: Charge = Protons - Électrons
Z = 11, donc 11 protons dans le noyau
Atome neutre Na: 11 protons, 11 électrons
Na → Na⁺ + 1e⁻ (perte de 1 électron)
Ion Na⁺: 11 protons, 10 électrons
Charge = 11 - 10 = +1
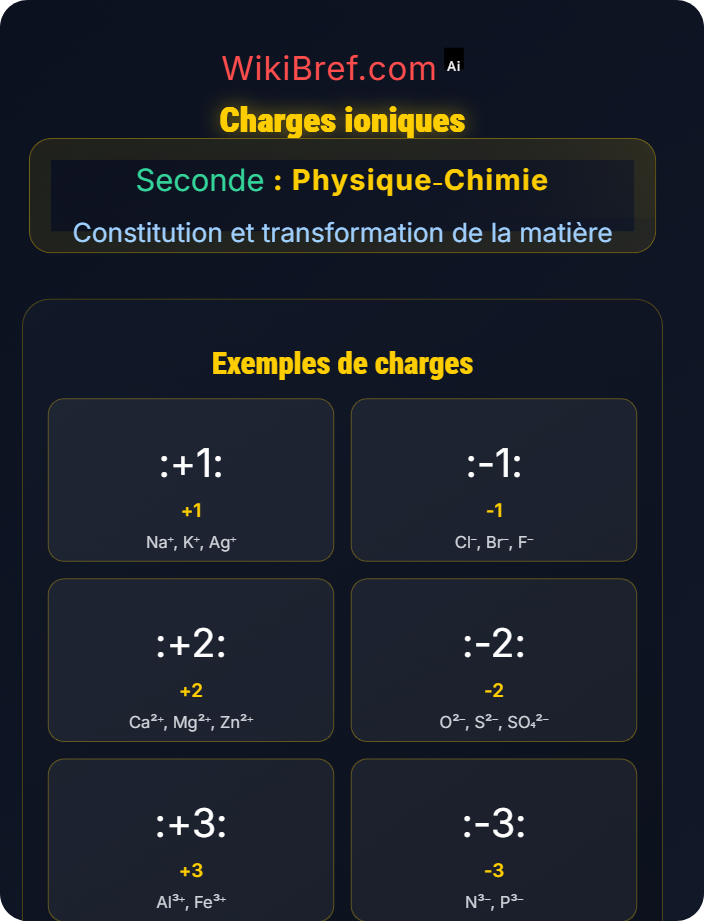
L'ion sodium Na⁺ a une charge de +1
• Charge = Protons - Électrons
• Numéro atomique Z = nombre de protons
• Perte d'électron → charge positive
Ion chlorure (Cl⁻) : Anion formé par gain d'un électron par l'atome de chlore.
Z = 17, donc 17 protons dans le noyau
Atome neutre Cl: 17 protons, 17 électrons
Cl + 1e⁻ → Cl⁻ (gain de 1 électron)
Ion Cl⁻: 17 protons, 18 électrons
Charge = 17 - 18 = -1
L'ion chlorure Cl⁻ a une charge de -1
• Charge = Protons - Électrons
• Gain d'électron → charge négative
• Numéro atomique Z = nombre de protons
Ion calcium (Ca²⁺) : Cation formé par perte de 2 électrons par l'atome de calcium.
Z = 20, donc 20 protons dans le noyau
Atome neutre Ca: 20 protons, 20 électrons
Ca → Ca²⁺ + 2e⁻ (perte de 2 électrons)
Ion Ca²⁺: 20 protons, 18 électrons
Charge = 20 - 18 = +2
L'ion calcium Ca²⁺ a une charge de +2
• Charge = Protons - Électrons
• Perte de 2 électrons → charge +2
• Numéro atomique Z = nombre de protons
Ion oxyde (O²⁻) : Anion formé par gain de 2 électrons par l'atome d'oxygène.
Z = 8, donc 8 protons dans le noyau
Atome neutre O: 8 protons, 8 électrons
O + 2e⁻ → O²⁻ (gain de 2 électrons)
Ion O²⁻: 8 protons, 10 électrons
Charge = 8 - 10 = -2
L'ion oxyde O²⁻ a une charge de -2
• Charge = Protons - Électrons
• Gain de 2 électrons → charge -2
• Numéro atomique Z = nombre de protons
Ion magnésium (Mg²⁺) : Cation formé par perte de 2 électrons de valence par l'atome de magnésium.
Z = 12, donc 12 protons dans le noyau
(K)²(L)⁸(M)², avec 2 électrons de valence
Mg → Mg²⁺ + 2e⁻ (perte des 2 électrons de valence)
Ion Mg²⁺: 12 protons, 10 électrons
Charge = 12 - 10 = +2
L'ion magnésium Mg²⁺ est formé par perte de 2 électrons, donnant une charge +2
• Charge = Protons - Électrons
• Électrons de valence → perte possible
• Perte de 2 électrons → charge +2
Ion aluminium (Al³⁺) : Cation formé par perte de 3 électrons de valence par l'atome d'aluminium.
Z = 13, donc 13 protons dans le noyau
(K)²(L)⁸(M)³, avec 3 électrons de valence
Al → Al³⁺ + 3e⁻ (perte des 3 électrons de valence)
Ion Al³⁺: 13 protons, 10 électrons
Charge = 13 - 10 = +3
L'ion aluminium Al³⁺ a une charge de +3
• Charge = Protons - Électrons
• Perte de 3 électrons → charge +3
• Numéro atomique Z = nombre de protons
Ion fluorure (F⁻) : Anion formé par gain d'un électron par l'atome de fluor.
Z = 9, donc 9 protons dans le noyau
(K)²(L)⁷, avec 7 électrons de valence
F + 1e⁻ → F⁻ (gain de 1 électron)
Ion F⁻: 9 protons, 10 électrons
Charge = 9 - 10 = -1
L'ion fluorure F⁻ a une charge de -1
• Charge = Protons - Électrons
• Gain d'électron → charge négative
• Numéro atomique Z = nombre de protons
Comparaison des charges : Différence entre les charges des ions K⁺ et Ca²⁺.
Z = 19, donc 19 protons, 18 électrons → charge +1
Z = 20, donc 20 protons, 18 électrons → charge +2
K⁺: charge +1, Ca²⁺: charge +2
Ca²⁺ a une charge plus élevée que K⁺
Ca²⁺ exerce une attraction plus forte sur les anions
L'ion Ca²⁺ a une charge +2 tandis que K⁺ a une charge +1
• Charge = Protons - Électrons
• Charge plus élevée → interaction plus forte
• Comparaison des charges → propriétés différentes
Ion sulfate (SO₄²⁻) : Ion polyatomique composé d'un atome de soufre et quatre atomes d'oxygène.
1 atome de soufre (S) + 4 atomes d'oxygène (O)
S: +6, O: -2 chacun (selon les règles d'oxydation)
Charge = (+6) + 4×(-2) = +6 - 8 = -2
SO₄²⁻ a une charge globale de -2
Requiert 2 cations monovalents ou 1 cation divalent pour neutralité
L'ion sulfate SO₄²⁻ a une charge de -2
• Charge globale = somme des charges partielles
• Ion polyatomique → charge collective
• Charge -2 → besoin de 2 charges positives pour neutralité
Charges multiples : Certains ions peuvent avoir des charges de +2, +3, -2, -3, etc.
Perte ou gain de plusieurs électrons de valence
Ca²⁺, Mg²⁺, Al³⁺, Fe²⁺/Fe³⁺
O²⁻, S²⁻, N³⁻, SO₄²⁻, PO₄³⁻
Configuration électronique, stabilité énergétique
Les charges multiples affectent la réactivité et la formation de composés
Les ions peuvent avoir des charges multiples selon leur configuration électronique et leur tendance à atteindre la stabilité
• Charges multiples → perte/gain de plusieurs électrons
• Stabilité → configuration électronique des gaz nobles
• Charges affectent → propriétés chimiques et formation de composés