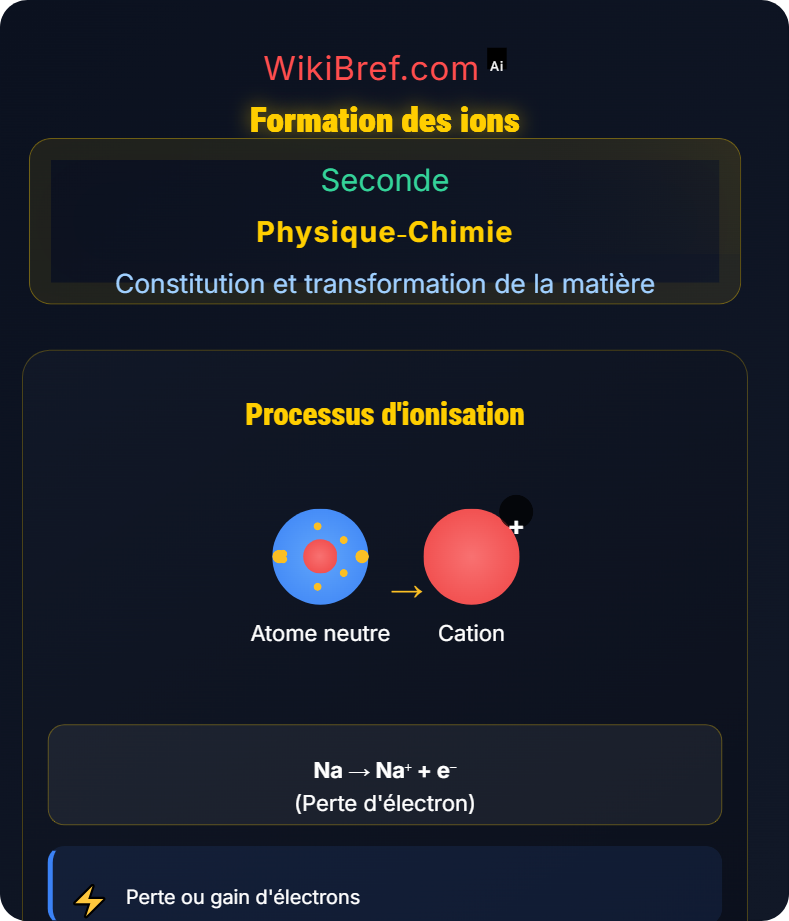
Mécanismes de formation
\( \text{Atome} \rightleftharpoons \text{Ion}^{n\pm} + n e^- \)
Perte ou gain d'électrons de valence
Na (K)²(L)⁸(M)¹
→
Na⁺ (K)²(L)⁸
+
+
e⁻
Cl (K)²(L)⁸(M)⁷
→
Cl⁻ (K)²(L)⁸(M)⁸
-
Formation du cation sodium:
Na → Na⁺ + e⁻
Perte de 1 électron externe
Perte de 1 électron externe
Formation de l'anion chlorure:
Cl + e⁻ → Cl⁻
Gain de 1 électron
Gain de 1 électron
Règles de stabilité
Règle de l'octet (8 e⁻)
Stabilité des gaz nobles
Les métaux perdent des e⁻
Les non-métaux gagnent des e⁻
Types d'ions
Cation monoatomique
Anion monoatomique
Anion polyatomique
Cation polyatomique
Conseils & Astuces
Regardez la configuration électronique
Les atomes cherchent la stabilité
Les alcalins forment des cations +
Les halogènes forment des anions -
Conservation de la charge électrique
Erreurs Fréquentes
Erreur 1 :
Confondre perte et gain d'électrons
Erreur 2 :
Ne pas respecter la règle de l'octet
Erreur 3 :
Oublier de vérifier la conservation de la charge