Définitions Clés
Nombre d'Avogadro (Nₐ) = 6,02 × 10²³ mol⁻¹
Relie la mole au nombre d'entités
Masse molaire (M) : Masse d'une mole de substance
Unité : g·mol⁻¹
Volume molaire (Vₘ) : Volume occupé par une mole
Dans les CNTP : Vₘ = 22,4 L·mol⁻¹
Échelles de grandeur :
1 mol = 6,02×10²³ entités
1 mol d'eau = 18,0 g
1 mol de gaz = 22,4 L (CNTP)
1 mol d'eau = 18,0 g
1 mol de gaz = 22,4 L (CNTP)
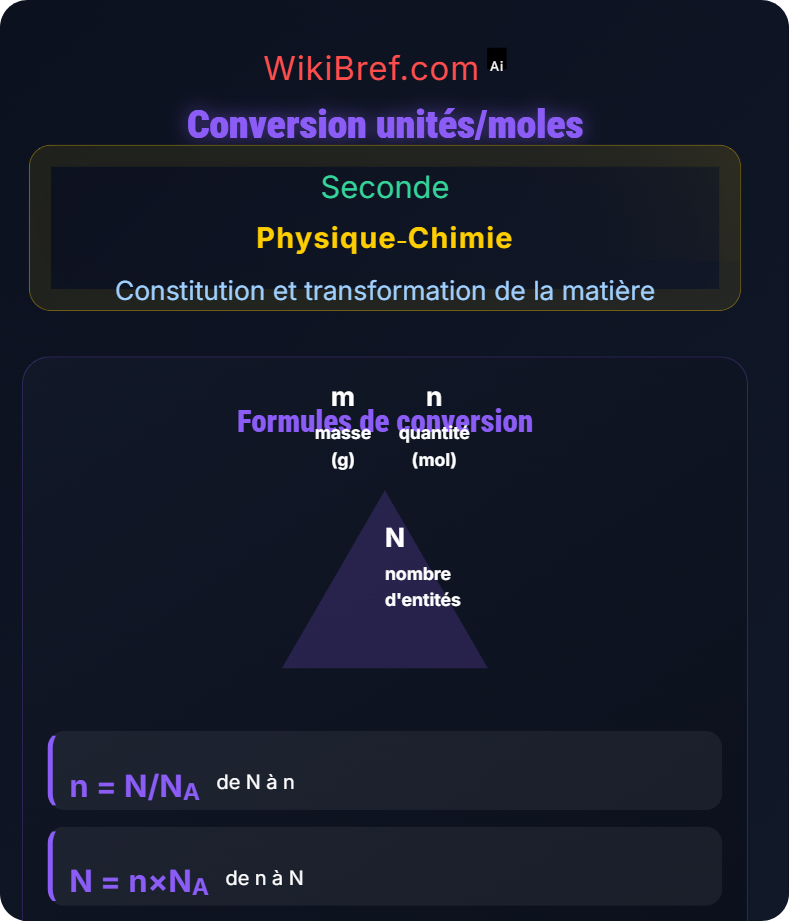
Formules de Conversion
\( n = \frac{N}{N_A} \)
De nombre d'entités à moles
\( N = n \times N_A \)
De moles à nombre d'entités
\( n = \frac{m}{M} \)
De masse à moles
\( n = \frac{V}{V_m} \)
De volume à moles (pour gaz)
Constantes à Connaître
N_A = 6,02×10²³ mol⁻¹
V_m = 22,4 L·mol⁻¹ (CNTP)
Les unités doivent être cohérentes
Méthodes de Conversion
Méthode 1 : Entités ↔ Moles
Utiliser N_A = 6,02×10²³
Division pour N→n
Multiplication pour n→N
Division pour N→n
Multiplication pour n→N
Méthode 2 : Masse ↔ Moles
Calculer M de la substance
Appliquer n = m/M ou m = n×M
Vérifier les unités
Appliquer n = m/M ou m = n×M
Vérifier les unités
Méthode 3 : Volume ↔ Moles (gaz)
Utiliser V_m = 22,4 L·mol⁻¹
n = V/V_m pour CNTP
Adapter selon conditions
n = V/V_m pour CNTP
Adapter selon conditions
Conseils & Astuces
Toujours vérifier les unités avant de calculer
Identifier le type de conversion demandée
Retenir les constantes importantes
Faire des conversions intermédiaires si nécessaire
Exemples Détaillés
Exemple 1 : Nombre → Moles
Combien de moles dans 1,20×10²⁴ atomes ?
n = N/N_A = 1,20×10²⁴ / 6,02×10²³ = 1,99 mol
n = N/N_A = 1,20×10²⁴ / 6,02×10²³ = 1,99 mol
Exemple 2 : Moles → Masse
Quelle masse pour 2,5 mol de glucose (C₆H₁₂O₆) ?
M = 6×12,0 + 12×1,0 + 6×16,0 = 180,0 g·mol⁻¹
m = n×M = 2,5×180,0 = 450 g
M = 6×12,0 + 12×1,0 + 6×16,0 = 180,0 g·mol⁻¹
m = n×M = 2,5×180,0 = 450 g
Exemple 3 : Volume → Moles (gaz)
Quelle quantité de matière dans 11,2 L de O₂ ?
n = V/V_m = 11,2 / 22,4 = 0,50 mol
n = V/V_m = 11,2 / 22,4 = 0,50 mol
Notes Clés à Retenir
✅ La mole est un pont entre le microscopique et le macroscopique
Elle permet de relier nombre d'entités, masse et volume
Elle permet de relier nombre d'entités, masse et volume
✅ N_A = 6,02×10²³ est une constante universelle
Elle sert à convertir entre entités et moles
Elle sert à convertir entre entités et moles
✅ Les formules de conversion sont à connaître par cœur
n=N/N_A, n=m/M, n=V/V_m
n=N/N_A, n=m/M, n=V/V_m
✅ Les unités doivent toujours être cohérentes
Convertir si nécessaire avant d'appliquer les formules
Convertir si nécessaire avant d'appliquer les formules
✅ Le volume molaire dépend des conditions physiques
22,4 L·mol⁻¹ seulement dans les CNTP
22,4 L·mol⁻¹ seulement dans les CNTP
Erreurs Fréquentes
Erreur 1 :
Oublier la notation scientifique pour N_A
Erreur 2 :
Confondre les différentes conversions
Erreur 3 :
Ne pas tenir compte des conditions pour le volume