Symbole nucléaire : \(^A_Z X\) où A = nombre de masse, Z = numéro atomique
- Identifier Z (numéro atomique) = nombre de protons
- Identifier A (nombre de masse) = protons + neutrons
- Calculer N (nombre de neutrons) = A - Z
- Pour un atome neutre, électrons = protons
\(^{12}_6C\) : A = 12, Z = 6
Protons = Z = 6
Neutrons = A - Z = 12 - 6 = 6
Électrons = Protons = 6 (atome neutre)
\(^{12}_6C\) contient 6 protons, 6 neutrons et 6 électrons
• A = Z + N
• Atome neutre : électrons = protons
• Z identifie l'élément
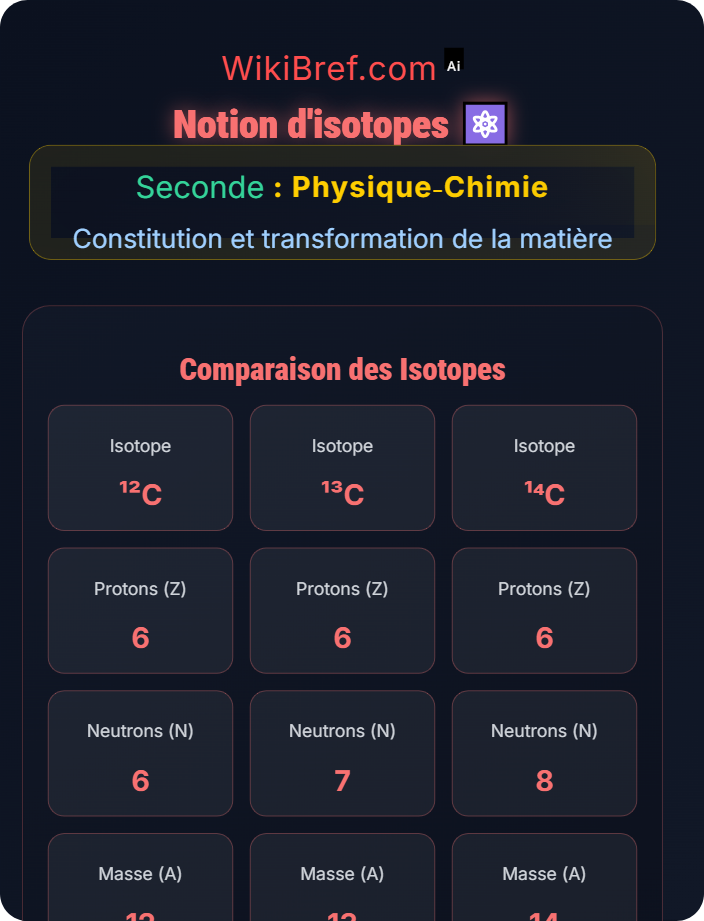
Isotopes : Atomes du même élément (même Z) mais avec des nombres de masse différents
\(^{12}_6C\) : Z = 6, A = 12
\(^{13}_6C\) : Z = 6, A = 13
\(^{14}_7N\) : Z = 7, A = 14
\(^{12}_6C\) et \(^{13}_6C\) ont Z = 6 → même élément (carbone)
\(^{14}_7N\) a Z = 7 → élément différent (azote)
\(^{12}_6C\) et \(^{13}_6C\) sont des isotopes du carbone
\(^{14}_7N\) n'est pas un isotope du carbone
\(^{12}_6C\) : 6 protons, 6 neutrons
\(^{13}_6C\) : 6 protons, 7 neutrons
\(^{12}_6C\) et \(^{13}_6C\) sont des isotopes du carbone car ils ont le même Z = 6 mais des A différents
• Isotopes : même Z, différents A
• Z détermine l'élément
• Affecte les propriétés physiques
Relation fondamentale : A = Z + N, donc N = A - Z
\(^{35}_{17}Cl\) : A = 35, Z = 17
Z = 17 → numéro atomique du chlore
N = A - Z = 35 - 17 = 18
Protons = 17, Neutrons = 18
Total = 17 + 18 = 35 = A ✓
\(^{37}_{17}Cl\) : N = 37 - 17 = 20 neutrons
\(^{35}_{17}Cl\) contient 18 neutrons
• N = A - Z
• Nombre de neutrons variable
• Isotopes naturels du chlore : ³⁵Cl (75%) et ³⁷Cl (25%)
Masse atomique moyenne : Moyenne pondérée des masses des isotopes naturels
³⁵Cl : abondance = 75,77%, masse = 34,969 u
³⁷Cl : abondance = 24,23%, masse = 36,966 u
³⁵Cl : 75,77% = 0,7577
³⁷Cl : 24,23% = 0,2423
\(\overline{M} = x_1 \cdot M_1 + x_2 \cdot M_2\)
\(\overline{M} = 0,7577 \times 34,969 + 0,2423 \times 36,966\)
\(\overline{M} = 26,496 + 8,956 = 35,452 u\)
Valeur tabulée : 35,45 u → très proche du calcul
La masse atomique moyenne du chlore est de 35,45 u
• \(\overline{M} = \sum x_i \cdot M_i\)
• Abondances naturelles constantes
• Explique les masses fractionnaires
Radioactivité : Désintégration spontanée du noyau pour atteindre une configuration plus stable
Pour une stabilité optimale, N/Z doit être proche d'une valeur idéale
Pour les légers : N ≈ Z, pour les lourds : N > Z
Ratio N/Z trop élevé ou trop faible
Trop de nucléons dans le noyau
Excès d'énergie
Bêta moins (β⁻) : conversion d'un neutron en proton
Bêta plus (β⁺) : conversion d'un proton en neutron
Alpha (α) : éjection de 2 protons + 2 neutrons
¹⁴C : instable, β⁻, T₁/₂ = 5730 ans
³H : instable, β⁻, T₁/₂ = 12,3 ans
Datation archéologique, médecine nucléaire, énergie nucléaire
Les isotopes radioactifs sont instables en raison d'un rapport neutron/proton inadéquat ou d'un excès d'énergie nucléaire
• Stabilité : N/Z optimal
• Désintégration : atteindre stabilité
• Applications : datation, médecine, énergie
Isotopes : Même Z, masses différentes en fonction du nombre de neutrons
¹⁶O : Z = 8, A = 16 → N = 16 - 8 = 8 neutrons
¹⁸O : Z = 8, A = 18 → N = 18 - 8 = 10 neutrons
Masse d'un proton ≈ 1,007 u
Masse d'un neutron ≈ 1,009 u
¹⁶O : 8 protons + 8 neutrons ≈ 8×1,007 + 8×1,009 ≈ 16,128 u
¹⁸O : 8 protons + 10 neutrons ≈ 8×1,007 + 10×1,009 ≈ 18,146 u
¹⁶O : 15,995 u
¹⁸O : 17,999 u
¹⁸O est plus lourd que ¹⁶O d'environ 2 u
L'isotope ¹⁸O est plus lourd que ¹⁶O car il possède 2 neutrons supplémentaires
• Masses isotopiques différentes
• Différence ≈ nombre de neutrons supplémentaires
• Applications : climatologie, études environnementales
Isotopes stables : Noyaux qui ne subissent pas de désintégration radioactive
Le carbone a plusieurs isotopes connus
¹²C : 98,93% - le plus abondant
¹³C : 1,07% - secondaire
¹⁴C : traces - radioactif, T₁/₂ = 5730 ans
¹²C : 6 protons, 6 neutrons
¹³C : 6 protons, 7 neutrons
¹⁴C : 6 protons, 8 neutrons
¹²C : standard pour la masse atomique
¹³C : RMN, études métaboliques
¹⁴C : datation archéologique
Les isotopes stables du carbone sont ¹²C (98,93%) et ¹³C (1,07%)
• Stabilité : rapport N/Z approprié
• Abondance naturelle variable
• Applications multiples selon l'isotope
Abondance naturelle : Proportion relative des isotopes dans la nature
Masse atomique du bore = 10,81 u
Isotopes : ¹⁰B et ¹¹B
Masses : ¹⁰B = 10,013 u, ¹¹B = 11,009 u
Soit x l'abondance de ¹⁰B, alors (1-x) celle de ¹¹B
10,81 = x×10,013 + (1-x)×11,009
10,81 = 10,013x + 11,009 - 11,009x
10,81 - 11,009 = 10,013x - 11,009x
-0,199 = -0,996x
x = 0,200 = 20,0%
¹¹B = 1 - 0,200 = 0,800 = 80,0%
0,200×10,013 + 0,800×11,009 = 2,003 + 8,807 = 10,81 u ✓
L'abondance naturelle du bore est : ¹⁰B (20,0%) et ¹¹B (80,0%)
• \(\overline{M} = \sum x_i \cdot M_i\)
• \(\sum x_i = 1\)
• Système d'équations pour résolution
Spectroscopie isotopique : Utilisation des différences de masse pour analyser la structure moléculaire
Différences de masse affectent les vibrations moléculaires
Fréquences d'absorption légèrement différentes
¹³C-RMN : analyse des carbones dans les molécules
²H (deutérium) : solvant en RMN (¹H)
¹²CO₂ et ¹³CO₂ ont des fréquences d'absorption différentes
Utilisé pour étudier les réactions enzymatiques
¹⁵N, ¹³C : traceurs en biochimie
Permettent de suivre les voies métaboliques
Études structurales, cinétiques chimiques, traçage métabolique
Les isotopes sont utilisés en spectroscopie pour étudier la structure et la dynamique des molécules grâce aux différences de masse
• Différences de masse = différences spectroscopiques
• Marquage isotopique = outil de suivi
• Applications : recherche fondamentale et médicale
Isotopes naturels de l'hydrogène : Protium, deutérium, tritium
¹H (protium) : 1 proton, 0 neutron, 99,985%
²H (deutérium) : 1 proton, 1 neutron, 0,015%
³H (tritium) : 1 proton, 2 neutrons, traces (radioactif)
\(\overline{M} = 0,99985×1,0078 + 0,00015×2,0141 + 0×3,0160\)
\(\overline{M} = 1,0077 + 0,000302 + 0 = 1,0080 u\)
Solvant en spectroscopie RMN
Études cinétiques (effet isotopique)
Recherche en fusion nucléaire
Deutérium : molécules plus lourdes, propriétés légèrement différentes
Exemple : H₂O vs D₂O (eau lourde)
Dans 1000 atomes d'hydrogène : 999,85 ¹H et 0,15 ²H
Un échantillon naturel d'hydrogène contient principalement ¹H (99,985%) et un peu de ²H (0,015%), avec des traces de ³H
• Abondances naturelles très variables
• Un seul proton dans tous les isotopes
• Applications importantes en recherche