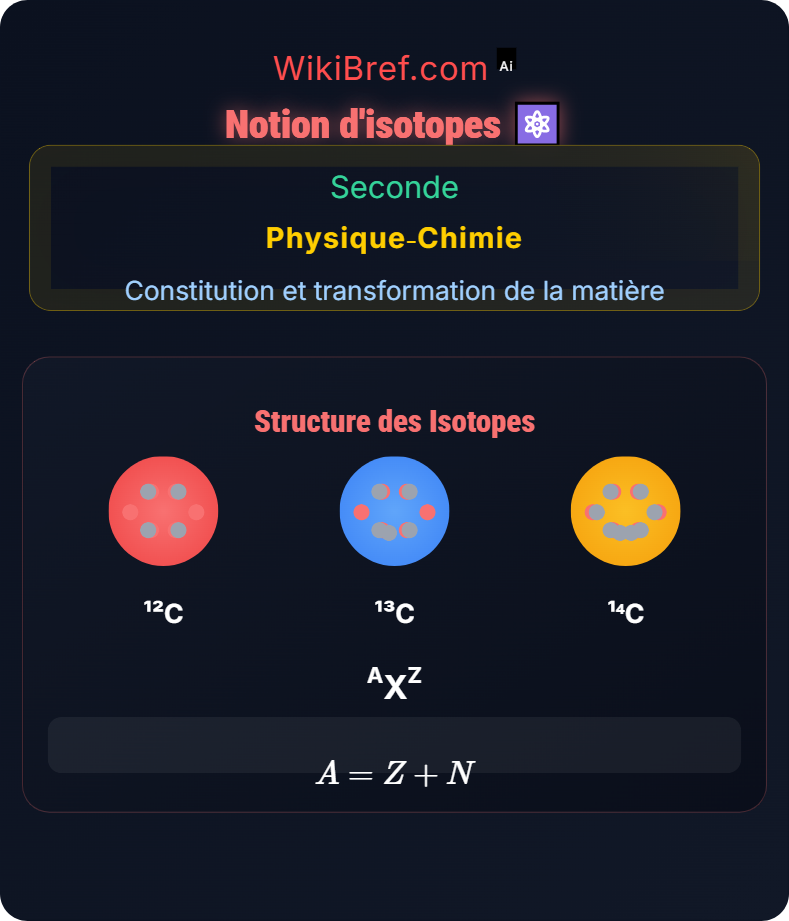
Isotopes
\( ^A_Z X \)
A = nombre de masse, Z = numéro atomique
Noyau
Carbone-12
Z = 6, A = 12
6p⁺, 6n⁰
Carbone-14
Z = 6, A = 14
6p⁺, 8n⁰
Exemples d'isotopes
Hydrogène: ¹H, ²H (deutérium), ³H (tritium)
Carbone: ¹²C, ¹³C, ¹⁴C
Oxygène: ¹⁶O, ¹⁷O, ¹⁸O
Carbone: ¹²C, ¹³C, ¹⁴C
Oxygène: ¹⁶O, ¹⁷O, ¹⁸O
Applications
Datation au carbone-14
Imagerie médicale
Études métaboliques
Imagerie médicale
Études métaboliques
Caractéristiques des isotopes
Même Z (protons), différent A (neutrons)
Mêmes propriétés chimiques
Masses différentes
Spectromètre de masse pour identification
Calcul de la masse atomique
\( m_{at} = \sum (x_i \times m_i) \)
xᵢ = abondance isotopique, mᵢ = masse isotopique
Exemple: Chlore
Isotope 35:
³⁵Cl : 75.77% d'abondance
Masse = 34.97 u
Masse = 34.97 u
Isotope 37:
³⁷Cl : 24.23% d'abondance
Masse = 36.97 u
Masse = 36.97 u
Masse atomique moyenne:
35.45 u
Conseils & Astuces
Tous les isotopes d'un élément ont le même Z
Nombre de neutrons = A - Z
Isotopes stables vs radioactifs
Seuls les protons déterminent l'élément
Abondance naturelle constante
Erreurs Fréquentes
Erreur 1 :
Confondre numéro atomique et nombre de masse
Erreur 2 :
Croire que les isotopes ont des propriétés chimiques différentes
Erreur 3 :
Oublier que Z détermine l'identité de l'élément
Stabilité des isotopes
Stables :
Ratio proton/neutron équilibré
Ex: ¹²C (stable)
Ex: ¹²C (stable)
Radioactifs :
Ratio instable → désintégration
Ex: ¹⁴C (radioactif)
Ex: ¹⁴C (radioactif)