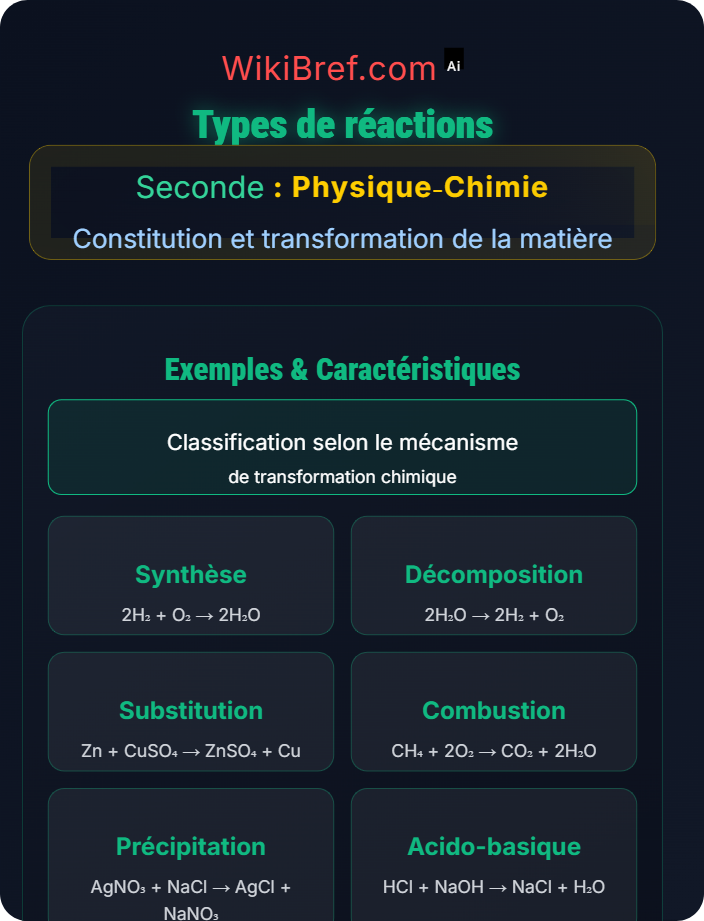
Réaction de synthèse : Combinaison de deux ou plusieurs substances simples pour former un composé plus complexe.
2 molécules de dihydrogène (H₂) et 1 molécule de dioxygène (O₂)
Ce sont des substances simples
2 molécules d'eau (H₂O)
C'est une substance plus complexe que les réactifs
Plusieurs réactifs simples → un produit complexe
Cette caractéristique correspond à une réaction de synthèse
Gauche : 4H, 2O
Droite : 4H, 2O
L'équation est équilibrée
Cette réaction est une synthèse.
Elle combine du dihydrogène et du dioxygène pour former de l'eau.
• Schéma général : A + B → AB
• Caractéristique : Plusieurs réactifs simples donnent un seul produit complexe
• Exemples : Formation de composés à partir d'éléments
Réaction de décomposition : Séparation d'un composé en deux ou plusieurs substances plus simples.
2 molécules d'eau (H₂O)
C'est une substance composée
2 molécules de dihydrogène (H₂) et 1 molécule de dioxygène (O₂)
Ce sont des substances simples
Un produit complexe → plusieurs réactifs simples
Cette caractéristique correspond à une réaction de décomposition
Gauche : 4H, 2O
Droite : 4H, 2O
L'équation est équilibrée
Cette réaction est une décomposition.
Elle sépare l'eau en dihydrogène et dioxygène.
• Schéma général : AB → A + B
• Caractéristique : Un seul réactif complexe donne plusieurs produits simples
• Conditions : Souvent nécessite de l'énergie (chaleur, électricité)
Réaction de substitution : Remplacement d'un atome ou d'un groupe d'atomes dans une molécule par un autre atome ou groupe.
Zn (zinc métallique) + CuSO₄ (sulfate de cuivre)
Le sulfate de cuivre contient Cu²⁺ et SO₄²⁻
ZnSO₄ (sulfate de zinc) + Cu (cuivre métallique)
Le sulfate de zinc contient Zn²⁺ et SO₄²⁻
Le zinc métallique remplace le cuivre dans le sulfate de cuivre
Zn remplace Cu dans CuSO₄ → ZnSO₄
Gauche : 1Zn, 1Cu, 1S, 4O
Droite : 1Zn, 1Cu, 1S, 4O
L'équation est équilibrée
Cette réaction est une substitution.
Le zinc remplace le cuivre dans le sulfate de cuivre.
• Schéma général : AB + C → AC + B
• Caractéristique : Un élément remplace un autre dans un composé
• Activité métallique : Le métal plus actif remplace le métal moins actif
Réaction d'addition : Combinaison de deux molécules pour former une seule molécule plus grande, souvent impliquant une liaison multiple.
C₂H₄ (éthylène) possède une double liaison C=C
H₂ (dihydrogène) est une molécule simple
C₂H₆ (éthane) n'a que des liaisons simples C-C et C-H
Le produit est saturé (pas de liaisons multiples)
La double liaison C=C est rompue
Les atomes d'hydrogène s'ajoutent aux carbones
Gauche : 2C, 6H
Droite : 2C, 6H
L'équation est équilibrée
Cette réaction est une addition.
Le dihydrogène s'ajoute à la double liaison de l'éthylène.
• Schéma général : AB + CD → ABCD
• Caractéristique : Liaison multiple → liaison simple
• Hydrogénation : Type spécifique d'addition avec H₂
Réaction d'échange (double) : Échange d'ions entre deux composés ioniques pour former deux nouveaux composés.
AgNO₃ → Ag⁺ + NO₃⁻
NaCl → Na⁺ + Cl⁻
AgCl → Ag⁺ + Cl⁻
NaNO₃ → Na⁺ + NO₃⁻
Les ions Ag⁺ et Na⁺ changent de partenaire
Les ions NO₃⁻ et Cl⁻ changent de partenaire
Gauche : 1Ag, 1N, 3O, 1Na, 1Cl
Droite : 1Ag, 1N, 3O, 1Na, 1Cl
L'équation est équilibrée
Cette réaction est une échange.
Les ions Ag⁺ et Na⁺ échangent leurs contre-ions.
• Schéma général : AB + CD → AD + CB
• Caractéristique : Échange d'ions entre composés
• Précipitation : Souvent forme un précipité (AgCl ici)
Réaction de synthèse : Combinaison de deux ou plusieurs substances simples pour former un composé plus complexe.
CaO (oxyde de calcium) et CO₂ (dioxyde de carbone)
Ce sont des substances simples comparées au produit
CaCO₃ (carbonate de calcium) est un composé plus complexe
Contient Ca²⁺, C⁴⁺ et O²⁻
Deux réactifs simples → un produit complexe
Cette caractéristique correspond à une réaction de synthèse
Gauche : 1Ca, 1C, 3O
Droite : 1Ca, 1C, 3O
L'équation est équilibrée
Cette réaction est une synthèse.
Elle combine l'oxyde de calcium et le dioxyde de carbone pour former du carbonate de calcium.
• Schéma général : A + B → AB
• Caractéristique : Plusieurs réactifs simples donnent un seul produit complexe
• Industrie : Réaction utilisée dans la production de ciment
Réaction de décomposition : Séparation d'un composé en deux ou plusieurs substances plus simples.
2KClO₃ (chlorate de potassium) est un composé complexe
Contient K⁺, Cl⁵⁺ et O²⁻
2KCl (chlorure de potassium) et 3O₂ (dihydrogène)
Ce sont des substances plus simples que le réactif
Un seul réactif complexe → plusieurs produits simples
Cette caractéristique correspond à une réaction de décomposition
Gauche : 2K, 2Cl, 6O
Droite : 2K, 2Cl, 6O
L'équation est équilibrée
Cette réaction est une décomposition.
Elle sépare le chlorate de potassium en chlorure de potassium et dioxygène.
• Schéma général : AB → A + B
• Caractéristique : Un seul réactif complexe donne plusieurs produits simples
• Catalyse : Souvent catalysée par MnO₂
Réaction de substitution : Remplacement d'un atome ou d'un groupe d'atomes dans une molécule par un autre atome ou groupe.
Cl₂ (dichlore) et 2KI (iodure de potassium)
KI contient K⁺ et I⁻
2KCl (chlorure de potassium) et I₂ (diode)
KCl contient K⁺ et Cl⁻
Le dichlore remplace l'iode dans l'iodure de potassium
Cl remplace I dans KI → KCl
Gauche : 2Cl, 2K, 2I
Droite : 2Cl, 2K, 2I
L'équation est équilibrée
Cette réaction est une substitution.
Le dichlore remplace l'iode dans l'iodure de potassium.
• Schéma général : AB + C → AC + B
• Halogènes : Cl₂ est plus réactif que I₂, donc remplace I₂
• Série d'activité : Cl > Br > I en termes de réactivité
Réaction d'addition : Combinaison de deux molécules pour former une seule molécule plus grande, souvent impliquant une liaison multiple.
CH₂=CH₂ (éthylène) possède une double liaison C=C
Br₂ (dibrome) est une molécule simple
CH₂Br-CH₂Br (1,2-dibromoéthane) n'a que des liaisons simples
Chaque carbone est maintenant lié à un atome de brome
La double liaison C=C est rompue
Les atomes de brome s'ajoutent aux carbones
Gauche : 2C, 4H, 2Br
Droite : 2C, 4H, 2Br
L'équation est équilibrée
Cette réaction est une addition.
Le dibrome s'ajoute à la double liaison de l'éthylène.
• Schéma général : AB + CD → ABCD
• Caractéristique : Liaison multiple → liaison simple
• Test halogène : Utilisée pour détecter les doubles liaisons
Réaction d'échange (double) : Échange d'ions entre deux composés ioniques pour former deux nouveaux composés.
BaCl₂ → Ba²⁺ + 2Cl⁻
Na₂SO₄ → 2Na⁺ + SO₄²⁻
BaSO₄ → Ba²⁺ + SO₄²⁻
2NaCl → 2Na⁺ + 2Cl⁻
Les ions Ba²⁺ et Na⁺ changent de partenaire
Les ions Cl⁻ et SO₄²⁻ changent de partenaire
Gauche : 1Ba, 2Cl, 2Na, 1S, 4O
Droite : 1Ba, 2Cl, 2Na, 1S, 4O
L'équation est équilibrée
Cette réaction est une échange.
Les ions Ba²⁺ et Na⁺ échangent leurs contre-ions.
• Schéma général : AB + CD → AD + CB
• Caractéristique : Échange d'ions entre composés
• Précipitation : BaSO₄ est très peu soluble, précipite