Définitions Clés
Équation chimique équilibrée : Représente une réaction chimique avec conservation des atomes
Coefficients stœchiométriques ajustés
Coefficient stœchiométrique : Nombre devant chaque espèce chimique
Indique la proportion de réaction
Loi de conservation : Les atomes ne sont ni créés ni détruits
Nombre identique d'atomes avant et après
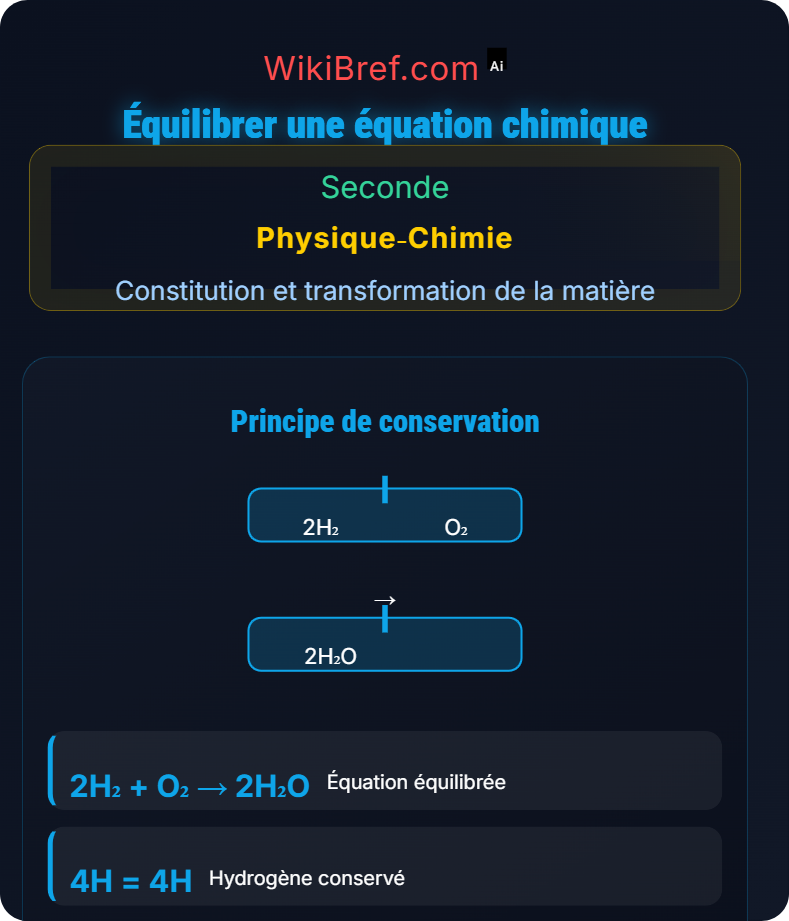
Exemple équilibré :
2H₂ + O₂ → 2H₂O
4H et 2O à gauche = 4H et 2O à droite
4H et 2O à gauche = 4H et 2O à droite
Règles de Conservation
Conservation des atomes
Même nombre d'atomes de chaque élément des deux côtés
Conservation de la charge
Somme des charges identiques des deux côtés (ions)
Conservation de la masse
Masse totale des réactifs = masse totale des produits
Méthodes d'équilibrage
Compter les atomes de chaque côté
Ajuster les coefficients
Vérifier la conservation
Méthodes d'équilibrage
Méthode 1 : Par inspection
Compter les atomes de chaque élément
Commencer par les éléments les plus complexes
Ajuster progressivement les coefficients
Vérifier la conservation finale
Commencer par les éléments les plus complexes
Ajuster progressivement les coefficients
Vérifier la conservation finale
Méthode 2 : Par système d'équations
Attribuer des variables aux coefficients
Écrire des équations pour chaque élément
Résoudre le système
Simplifier au plus petit entier
Écrire des équations pour chaque élément
Résoudre le système
Simplifier au plus petit entier
Conseils & Astuces
Commencer par les atomes qui n'apparaissent qu'une fois
Traiter les molécules complexes en dernier
Vérifier toujours la charge totale
Utiliser des fractions temporairement si nécessaire
Exemples Détaillés
Exemple 1 : Combustion du méthane
CH₄ + O₂ → CO₂ + H₂O
Étape 1 : C équilibré (1 de chaque côté)
Étape 2 : H : 4 à gauche → 2H₂O à droite
Étape 3 : O : 2 à gauche → 2CO₂ + 2H₂O → 4O
Équation finale : CH₄ + 2O₂ → CO₂ + 2H₂O
Étape 1 : C équilibré (1 de chaque côté)
Étape 2 : H : 4 à gauche → 2H₂O à droite
Étape 3 : O : 2 à gauche → 2CO₂ + 2H₂O → 4O
Équation finale : CH₄ + 2O₂ → CO₂ + 2H₂O
Exemple 2 : Synthèse de l'ammoniac
N₂ + H₂ → NH₃
Étape 1 : 2N à gauche → 2NH₃ à droite
Étape 2 : 6H à droite → 3H₂ à gauche
Équation finale : N₂ + 3H₂ → 2NH₃
Étape 1 : 2N à gauche → 2NH₃ à droite
Étape 2 : 6H à droite → 3H₂ à gauche
Équation finale : N₂ + 3H₂ → 2NH₃
Exemple 3 : Réaction acido-basique
HCl + NaOH → NaCl + H₂O
Déjà équilibrée : 1H, 1Cl, 1Na, 1O de chaque côté
Déjà équilibrée : 1H, 1Cl, 1Na, 1O de chaque côté
Notes Clés à Retenir
✅ Les coefficients ajustent les proportions, pas les formules
On ne modifie jamais les indices dans les formules
On ne modifie jamais les indices dans les formules
✅ La conservation des atomes est absolue
Chaque atome doit être comptabilisé de chaque côté
Chaque atome doit être comptabilisé de chaque côté
✅ Les coefficients doivent être les plus petits entiers possibles
Simplifier si tous les coefficients ont un facteur commun
Simplifier si tous les coefficients ont un facteur commun
✅ La charge électrique doit aussi être conservée
Particulièrement important pour les réactions ioniques
Particulièrement important pour les réactions ioniques
✅ L'équilibrage est une compétence fondamentale
Nécessaire pour tous les calculs stœchiométriques
Nécessaire pour tous les calculs stœchiométriques
Erreurs Fréquentes
Erreur 1 :
Modifier les indices dans les formules chimiques
Erreur 2 :
Oublier de vérifier la conservation des charges
Erreur 3 :
Ne pas simplifier les coefficients au plus petit entier