Configuration électronique
\( K-L-M-N-O-P-Q \)
Couches électroniques
K (2 e⁻)
L (8 e⁻)
M (18 e⁻)
Exemple Carbone (Z=6):
6 électrons
Configuration: (K)²(L)⁴
Configuration: (K)²(L)⁴
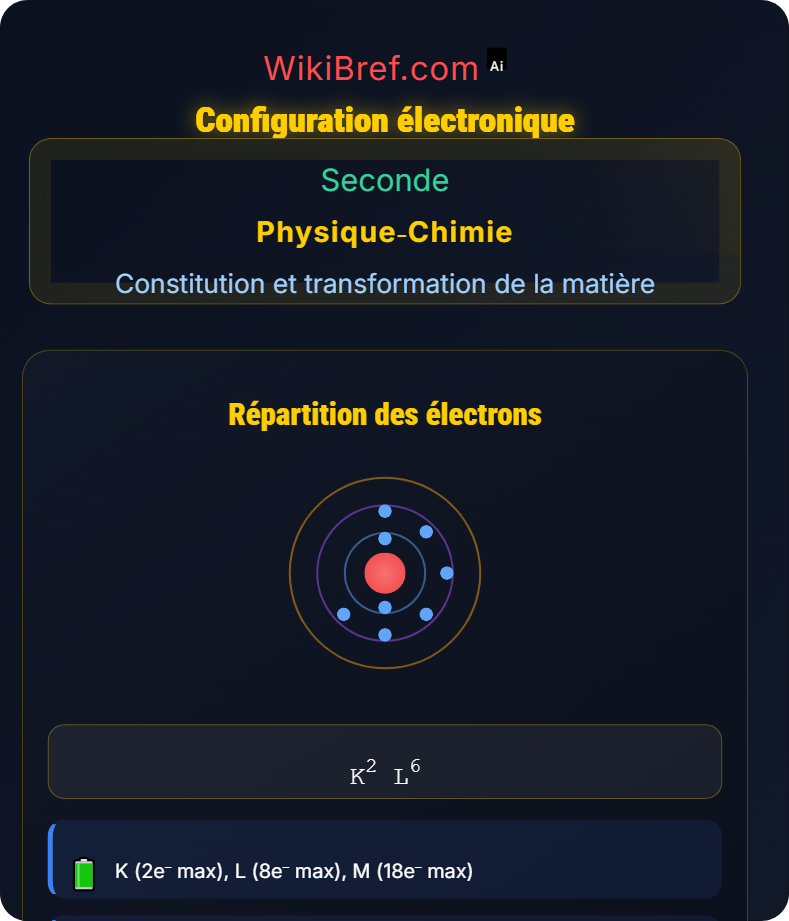
Exemple Oxygène (Z=8):
8 électrons
Configuration: (K)²(L)⁶
Configuration: (K)²(L)⁶
Règles de remplissage
Ordre: K → L → M → N...
Capacité max: 2n² électrons
Couche externe: électrons de valence
Électrons = protons dans atome neutre
Capacités maximales
K: 2 électrons maximum
L: 8 électrons maximum
M: 18 électrons maximum
N: 32 électrons maximum
Conseils & Astuces
Compter les électrons de l'extérieur vers l'intérieur
Les électrons de valence déterminent la réactivité
Règle de l'octet: tendance à avoir 8 e⁻ externes
Les gaz nobles ont une couche externe complète
Notation: (K)²(L)⁸(M)¹ pour Na
Erreurs Fréquentes
Erreur 1 :
Dépasser la capacité maximale d'une couche
Erreur 2 :
Inverser l'ordre de remplissage
Erreur 3 :
Confondre électrons de valence et électrons totaux