Définitions Clés
Masse molaire (M) : Masse d'une mole de substance
Unité : g·mol⁻¹ ou kg·mol⁻¹
Masse molaire atomique : Masse d'une mole d'atomes
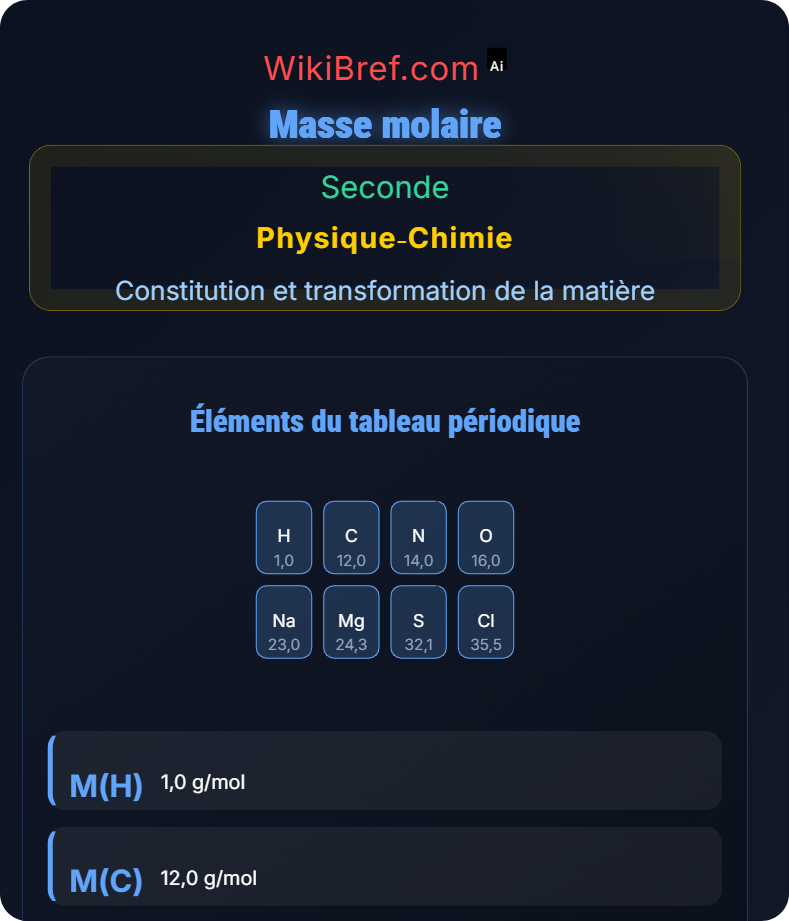
Valeurs données dans le tableau périodique
Masse molaire moléculaire : Somme des masses molaires des atomes
Calculée à partir de la formule chimique
Exemples :
M(C) = 12,0 g·mol⁻¹
M(H) = 1,0 g·mol⁻¹
M(O) = 16,0 g·mol⁻¹
M(H) = 1,0 g·mol⁻¹
M(O) = 16,0 g·mol⁻¹
Formules Essentielles
\( M = \frac{m}{n} \)
M : masse molaire (g·mol⁻¹)
m : masse (g)
n : quantité de matière (mol)
m : masse (g)
n : quantité de matière (mol)
\( m = n \times M \)
Calcul de la masse à partir de n et M
\( n = \frac{m}{M} \)
Calcul de la quantité de matière à partir de m et M
Règles de Calcul
Pour une molécule : somme des M des atomes
Toujours respecter les proportions stœchiométriques
Multiplier par le nombre d'atomes dans la molécule
Méthodes de Calcul
Méthode 1 : Calcul M d'une molécule
Étape 1 : Identifier la formule chimique
Étape 2 : Repérer chaque type d'atome
Étape 3 : Multiplier chaque M par son coefficient
Étape 4 : Faire la somme
Étape 2 : Repérer chaque type d'atome
Étape 3 : Multiplier chaque M par son coefficient
Étape 4 : Faire la somme
Méthode 2 : Calcul de masse à partir de n
Étape 1 : Identifier n et M
Étape 2 : Appliquer m = n × M
Étape 3 : Vérifier les unités
Étape 2 : Appliquer m = n × M
Étape 3 : Vérifier les unités
Conseils & Astuces
Toujours noter les unités dans vos calculs
Utiliser le tableau périodique pour les valeurs de M
Ne pas confondre masse molaire et masse réelle
Faire attention aux parenthèses dans les formules
Exemples Détaillés
Exemple 1 : Calcul de M(H₂O)
M(H₂O) = 2×M(H) + M(O)
M(H₂O) = 2×1,0 + 16,0 = 18,0 g·mol⁻¹
M(H₂O) = 2×1,0 + 16,0 = 18,0 g·mol⁻¹
Exemple 2 : Calcul de M(C₆H₁₂O₆)
M(C₆H₁₂O₆) = 6×M(C) + 12×M(H) + 6×M(O)
M(C₆H₁₂O₆) = 6×12,0 + 12×1,0 + 6×16,0 = 180,0 g·mol⁻¹
M(C₆H₁₂O₆) = 6×12,0 + 12×1,0 + 6×16,0 = 180,0 g·mol⁻¹
Exemple 3 : Calcul de la masse
Quelle masse pour 2,5 mol de NaCl ?
M(NaCl) = M(Na) + M(Cl) = 23,0 + 35,5 = 58,5 g·mol⁻¹
m = n×M = 2,5×58,5 = 146,25 g
M(NaCl) = M(Na) + M(Cl) = 23,0 + 35,5 = 58,5 g·mol⁻¹
m = n×M = 2,5×58,5 = 146,25 g
Notes Clés à Retenir
✅ La masse molaire est caractéristique d'une espèce chimique
Elle ne dépend pas de la quantité de matière
Elle ne dépend pas de la quantité de matière
✅ Unité : g·mol⁻¹ (grammes par mole)
Parfois kg·mol⁻¹ dans certains contextes
Parfois kg·mol⁻¹ dans certains contextes
✅ Formules à connaître par cœur
M = m/n, m = n×M, n = m/M
M = m/n, m = n×M, n = m/M
✅ Pour une molécule : additionner les M des atomes
Ne pas oublier les coefficients stœchiométriques
Ne pas oublier les coefficients stœchiométriques
✅ La masse molaire relie masse et quantité de matière
C'est un pont entre le monde macroscopique et microscopique
C'est un pont entre le monde macroscopique et microscopique
Erreurs Fréquentes
Erreur 1 :
Oublier de multiplier par le nombre d'atomes dans la molécule
Erreur 2 :
Confondre masse molaire et masse réelle
Erreur 3 :
Mauvaise utilisation des formules de conversion