Définitions Clés
Mole (mol) : Unité de quantité de matière
Contient exactement 6,02 × 10²³ entités élémentaires
Nombre d'Avogadro (Nₐ) = 6,02 × 10²³ mol⁻¹
Constante universelle liant mole et nombre d'entités
Exemple :
1 mol de carbone contient 6,02 × 10²³ atomes de carbone
1 mol d'eau contient 6,02 × 10²³ molécules H₂O
1 mol d'eau contient 6,02 × 10²³ molécules H₂O
Ordre de grandeur :
6,02 × 10²³ ≈ 602 000 000 000 000 000 000 000
C'est un nombre astronomique !
C'est un nombre astronomique !
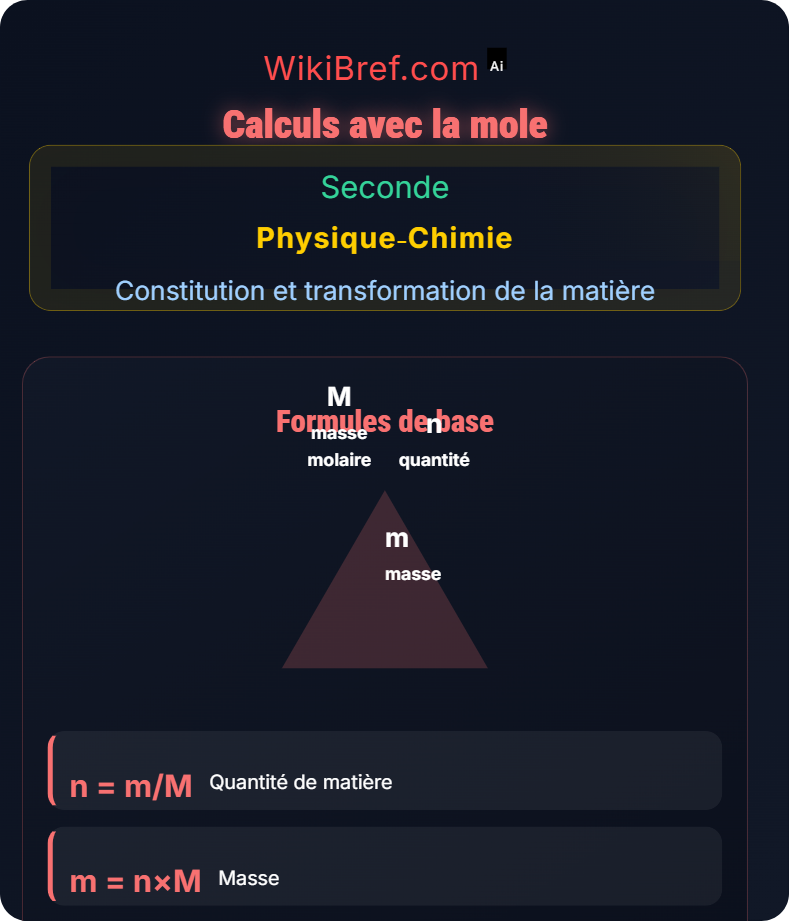
Formules Essentielles
\( n = \frac{N}{N_A} \)
n : quantité de matière (mol)
N : nombre d'entités
N_A : nombre d'Avogadro
N : nombre d'entités
N_A : nombre d'Avogadro
\( N = n \times N_A \)
Formule inverse pour retrouver le nombre d'entités
Règles de Conversion
Multiplier pour passer de mol à entités
Diviser pour passer d'entités à mol
Toujours utiliser N_A = 6,02 × 10²³
Méthodes de Calcul
Méthode 1 : De mol à entités
Étape 1 : Identifier n (quantité de matière)
Étape 2 : Multiplier par N_A
Étape 3 : Arrondir au bon nombre de chiffres significatifs
Étape 2 : Multiplier par N_A
Étape 3 : Arrondir au bon nombre de chiffres significatifs
Méthode 2 : D'entités à mol
Étape 1 : Identifier N (nombre d'entités)
Étape 2 : Diviser par N_A
Étape 3 : Exprimer en notation scientifique si nécessaire
Étape 2 : Diviser par N_A
Étape 3 : Exprimer en notation scientifique si nécessaire
Conseils & Astuces
Toujours vérifier les unités dans vos calculs
Lire attentivement l'énoncé pour identifier n ou N
Utiliser la proportionnalité directe
Pratiquer avec des exemples concrets
Exemples Détaillés
Exemple 1 : Calculer N à partir de n
Combien d'atomes dans 2,5 mol de fer ?
N = n × N_A = 2,5 × 6,02×10²³ = 1,51×10²⁴ atomes
N = n × N_A = 2,5 × 6,02×10²³ = 1,51×10²⁴ atomes
Exemple 2 : Calculer n à partir de N
Quelle quantité de matière pour 3,01×10²³ molécules d'eau ?
n = N/N_A = 3,01×10²³ / 6,02×10²³ = 0,50 mol
n = N/N_A = 3,01×10²³ / 6,02×10²³ = 0,50 mol
Exemple 3 : Calcul de masse molaire
M(H₂O) = 2×M(H) + M(O) = 2×1,0 + 16,0 = 18,0 g/mol
Notes Clés à Retenir
✅ La mole est une unité de quantité de matière
Elle permet de compter des entités microscopiques
Elle permet de compter des entités microscopiques
✅ N_A = 6,02 × 10²³ est une constante universelle
Toujours la même valeur dans tous les calculs
Toujours la même valeur dans tous les calculs
✅ Formules à connaître par cœur
n = N/N_A et N = n×N_A
n = N/N_A et N = n×N_A
✅ Attention aux unités
n en mol, N est sans unité, N_A en mol⁻¹
n en mol, N est sans unité, N_A en mol⁻¹
✅ La mole facilite les calculs chimiques
Elle relie le monde microscopique au monde macroscopique
Elle relie le monde microscopique au monde macroscopique
Erreurs Fréquentes
Erreur 1 :
Confondre la mole avec la masse
Erreur 2 :
Oublier la notation scientifique pour N_A
Erreur 3 :
Inverser les formules de conversion